呉須の色は酸化コバルトの働きにより、青く見えています。
釉薬では、例えば赤色はセレン赤 (CdS-CdSe)、ピンク色の釉薬は陶試紅(Al2O3(Mn・P))、青磁は鉄、織部釉は銅の働きによって色づいています。
さて、色はどの様にして見えているのでしょうか。
まず、対象物に光が当たり、その光を反射(吸収)します。
その光が私たちの網膜に入り込むことで私たちは物の色を認識しているのです。
なお、私たちが認識できる色は可視光線と呼ばれます。
それ以外の光は赤外線や紫外線と呼ばれます。
今回は、吸収された光がどうなっているのかをご説明いたします。
Table of Contents
原子スペクトル
原子スペクトルとは原子が放射または吸収する光のスペクトルのことを言います。
スペクトルとは簡単に言うと電磁波のことです。
専門的には分光器(プリズムや回折格子など)を通すことによって得られる、電磁波の波長ごとの強度分布を記録したものという表現になります。
この波は光が原子に当たった際に吸収したエネルギーを放出するものです。
まず、原子の説明をします。
原子とは
原子とは、物質を構成する基本的な最小構成単位となっている粒子のことです。
大まかに陽子・中性子・電子で構成されています。
この中で電子の動きが色と大きく関係しています。
例えば、ナトリウム原子の場合、11+の電荷を持った原子核(陽子・中性子)とその周りに11個の電子があります。この電子は原子核の周りを絶えずぐるぐると回っています。
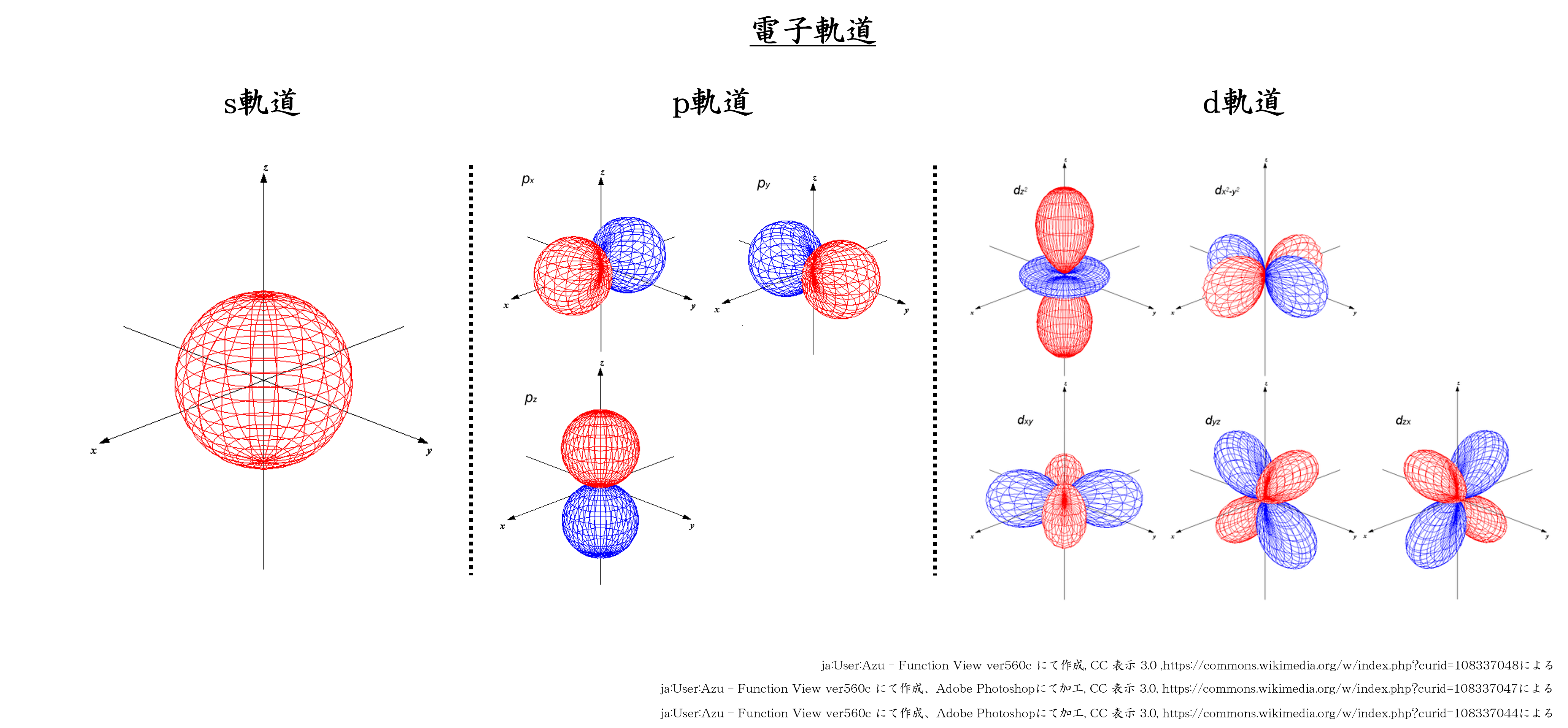
電子の電子軌道
このぐるぐる回る軌道には種類があり、内側から種類別にs軌道、p起動、d軌道と呼びます(他にも種類があります)。
ナトリウム原子では1s軌道に2個、2s軌道に2個、2p軌道に6個、3s軌道に1個電子が入っています。
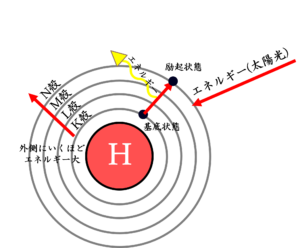
基底状態と励起状態
この通常の軌道に電子が入っている状態を基底状態といいます。
原子にエネルギーが与えられると、一番外側の電子軌道にある電子がその他の軌道に移動します。この時の状態を励起状態といいます。
基底状態の電子軌道は原子別に一つに決まります。一方、励起状態は電子が色々な軌道に移動するので、複数の電子軌道があります。ただ、基底状態と励起状態のエネルギー差は常に一定の値となります。
この励起状態はエネルギーの高い状態で不安定です。なので、安定している基底状態に戻ります。
この基底状態に戻る際に原子は吸収したエネルギー分を電磁波として放出します。
これが原子スペクトルと呼ばれるものです。
そして、基底状態と励起状態のエネルギー差は常に一定であることから、原子別には常に一定のエネルギーを放出します。
例えば、ナトリウム原子の基底状態のエネルギーは2.103eV、励起状態のエネルギーは2.105eVです。
これを波長に換算すると589.0nmと589.6nmです。これがナトリウムランプが黄色く光る原因です。
この基底状態と励起状態のエネルギー差は原子別に原子固有であり、それぞれの原子スペクトルを放出します。
まとめ
今回は原子スペクトルに関するメカニズムをご説明しました。
おさらいをすると原子にエネルギーを与えると、原子がそのエネルギーを吸収して基底状態から励起状態となります。
この励起状態から基底状態に戻る際に放出する電磁波を原子スペクトルと呼びます。
呉須釉薬についてのご相談は、深海商店にお気軽にご相談ください。









